圖說:陽明交大與國衛院團隊找出阿茲海默新關鍵,右起國衛院主任謝世良、陽明交大腦科所副教授鄭菡若、林鈺益博士生。
CLEC5A基因所轉譯的蛋白是存在於免疫細胞中的一種受體,過去研究指出在登革熱、日本腦炎、流感甚至新冠病毒感染時,會促使免疫系統產生強烈的發炎反應,有時甚至導致致命的「細胞激素風暴」。陽明交大腦科學研究所副教授鄭菡若,與國家衛生研究院免疫醫學研究中心主任謝世良領軍的團隊,首次揭露這個與病毒感染息息相關的基因,竟也參與了阿茲海默症的發展過程。
研究團隊透過基因工程,將阿茲海默症小鼠與剔除了CLEC5A基因的小鼠進行育種。跟有記憶缺失的阿茲海默症小鼠相比,那些缺少CLEC5A基因的阿茲海默症小鼠在記憶與學習的行為測試中表現顯著提升,大腦中β類澱粉蛋白的堆積也大幅減少——這些蛋白正是阿茲海默症的關鍵病理指標。
鄭菡若表示,微膠細胞(microglia)是腦神經重要的免疫細胞,但阿茲海默症的β類澱粉蛋白異常堆積,也會引發微膠細胞不正常活化而攻擊腦神經。剔除CLEC5A基因後不僅降低微膠細胞的發炎活性,也同時提高對β類澱粉蛋白的清除能力。這意味著CLEC5A基因可能是為治療阿茲海默症的新的治療標的。
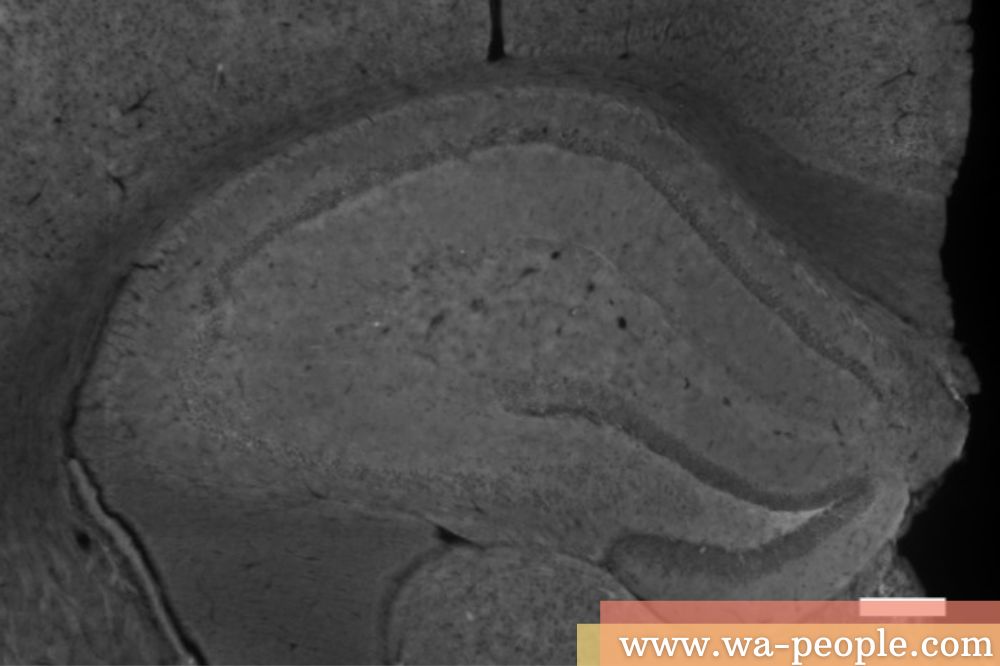
圖說:阿茲海默小鼠海馬迴的斑塊堆積情形
「當時只是猜測,還沒有明顯證據。」發現CLEC5A是登革熱與日本腦炎致死重要因子的謝世良,一開始對於這個基因與阿茲海默症的關聯也沒有絕對把握。他說,CLEC5A不只會辨認病毒,後來在紅斑性狼瘡等自體免疫疾病中也有表現,「所以我們當時就在猜測,這個基因是不是也在阿茲海默症裡誤傷大腦。」
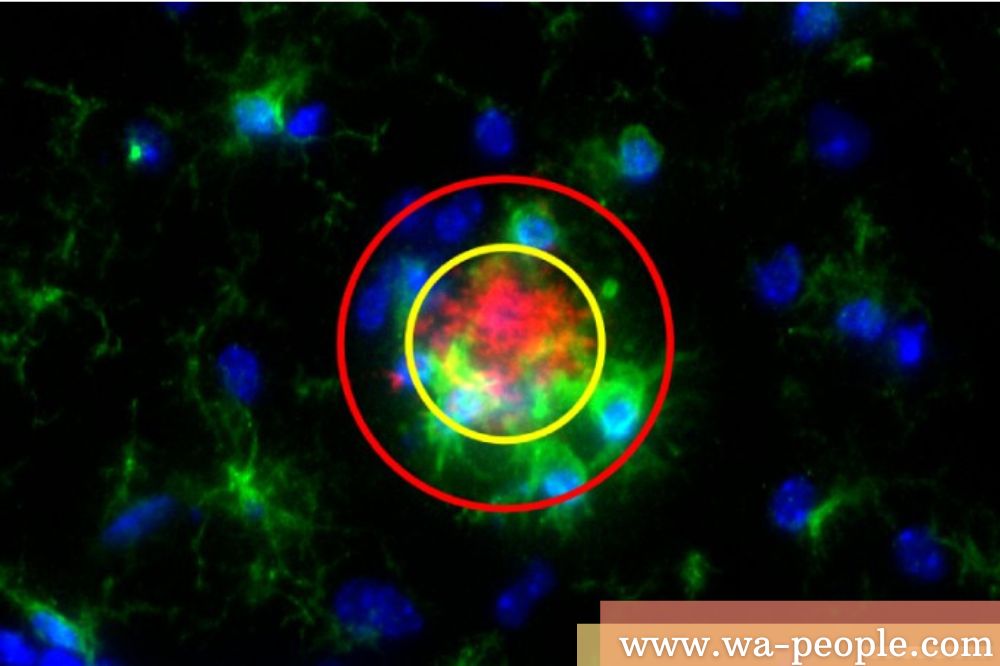
圖說:阿茲海默小鼠海馬迴迴微膠細胞關聯的斑塊區域,黃圈為涵蓋所有斑塊,紅圈為半徑放大10微米後的關聯區域。
這項研究也有陽明交大腦科所林鈺益與張文瀚兩位博士生的重要參與,成果已發表於國際期刊《Journal of Neuroinflammation》。不僅揭示病毒感染基因在神經退化疾病中的新角色,也點出未來以藥物阻斷CLEC5A蛋白功能作為阿茲海默症治療的新可能。
















